Общие закономерности концентрации и распространения РЗЭ.
Сдерживающая родительская литологическая и петрогенетическая среда гор обеспечивает при процессах плавления различия в общем количестве и распределении элементов всего класса, но не все интерпретации этого сложны. Во-первых, как отмечалось ранее, какая-либо степень плавления и сортировки будет результировать, главным образом, обогащенными РЗЭ в продуктах самых низких температур плавления и наиболее подвижных вулканических горных породах. Как результат, общая структура может быть рассмотрена во всей солнечной системе. Свободный Cl в большом количестве представлен в Солнечной системе. Твердые планеты обогащены этими хлорными хондритами. Кора скальных планет более обогащена, чем мантия. Высоко распределенные кислые породы сильнее обогащены по сравнению с их мафитовыми и ультра-мафитовыми прародителями и т.д.
Вторая главная тенденция в поведении РЗЭ – это то, как они взаимодействуют с исходными и производными объемами горных пород, общее обогащение или обеднение тяжелых РЗЭ относительно легких. К тяжелым относится группа элементов от тербия до лютеция. Элементы, относящиеся к тяжелым, обладают большей атомной массой. Легкие РЗЭ – от лантана до гадолиния. Они обладают меньшей атомной массой. По мере возрастания атомного номера РЗЭ наблюдается хоть и небольшое, но устойчивое снижение ионного радиуса. Несмотря на то, что изменение несущественно, оно создает ощутимый эффект на совместимость РЗЭ, обусловленную меньшим или большим атомным номером. Иными словами, так как тяжелые РЗЭ меньше по размерам, они лучше включены в кристаллическую решетку формирующих силикатов, чем легкие РЗЭ. Это значит, что они, по сравнению с легкими РЗЭ, обедняют формирующиеся впоследствии породы, что сильно изменит распределение РЗЭ в пользу светлого конца спектра. Крайнее проявление этого – в появлении силикатов гранатового цвета, в которых тяжелые РЗЭ высоко совместимы с любыми стандартами.
Третья главная тенденция в использовании РЗЭ для интерпретации вулканических петрогенетических отношений – это разработка аномалии европия в его ответе на кристаллизацию плагиоклаза. Хотя эта функция очень специфична, она заметна в таком большом проценте участков РЗЭ, что трудно ее недооценить. Европий, как отмечалось выше, способен менять заряженность с +3, характерной для всех РЗЭ, на +2, путем присоединения одного валентного электрона. Как результат, европий может замещать кальций в плагиоклазовых кристаллических решетках. Плагиоказовый полевой шпат – один из самых распространенных минералов каменных участков Солнечной системы. Температуры его кристаллизации и плавления умеренные, поэтому он – частый участник процессов плавления и кристаллизации горных пород на протяжении вулканических процессов. Так как плагоклаз изолирует европий в своих кристаллических решетках, породы, кристаллизованые из расплавленной массы, после того, как плагиоклаз был кристаллизован в достаточно больших количествах, будут показывать снижение уровня РЗЭ, из которых извлечен европий. Также расплав, который включает в себя первично кристаллизованный плагиоказ, может показать возрастающее количество европия в сравнении с уровнем других РЗЭ. Суммируя все это, можно сказать, что если в процесс кристаллизации включен плагиоклаз , то будет наблюдаться положительный (плавление) или отрицательный (кристаллизация) рост аномалии европия.
Эти три примера только часть из возможных способов, при которых тонкие различия в ионном радиусе или заряженности могут провоцировать большие различия в совместимости минералов и последующих элементных коэффициентов распределения. Эти типы различений делаю РЗЭ очень чувствительным инструментом для рассмотрения и понимания дифференциации на всех уровнях – от планетарного до очень локального.
Запасы редкоземельных элементов
Общее количество по массе редкоземельных металлов в природе составляет не более 0,02%. Чаще всего в недрах Земли находятся церий, лантан и неодим. Наименее распространенным соединением является Европий. Ее процентное содержание в недрах Земли составляет не более 0,0013% от его общей массе.

В мире редкоземельные металлы находятся в 240 минеральных веществах: фторидах, силикатах и фосфатах. 62 минерала используются в качестве промышленного сырья: монацит, апатит, бастнезит и эвксенит. Процентное соотношение РЗЭ в составе минеральных веществ неодинаково. В бастнезитах содержатся преимущественно представители цериевой подгруппы, в апатитах – иттриевой.
Редкоземельные элементы содержаться в естественной среде совместно, образуя сульфиды или галоидные соединения. Валентность веществ составляет не более 3+. В природе церий может образовывать четырехвалентные соединения, что обусловлено особенностями строения его электронной оболочки.
Основные запасы редкоземельных металлов содержатся в следующих странах:
- США: 13000000 т;
- Австралия: 1600000 т;
- Бразилия: 36000 т;
- Китай: 55000000 т;
- Индия: 3100000 т;
- Малайзия: 30000 т.
https://youtube.com/watch?v=NQINNHoiGiE
В России 90% редкоземельных элементов импортируется из других стран. Это обусловлено тем, что на российском рынке наблюдается низкий спрос на данные соединения. Из-за развития научно-технического прогресса наибольшее количество редкоземельных ресурсов потребляется развитыми странами Европы и Северной Америки.
Использование редкоземельных металлов
Редкоземельные элементы (РЗЭ) представляют собой очень востребованную на сегодняшний день группу элементов. Их используют во многих областях, активно развивающихся в настоящее время.
Очень сложно переоценить значение данных веществ. Новые исследования позволяют предположить, что развитие технологий с применением РЗЭ позволять снизить или даже полностью ликвидировать энергетическую зависимость государств. На их основе разрабатываются технологии будущего в таких сферах как, здравоохранение, оборона, компьютерная промышленность и всевозможные гаджеты для связи. К тому же они позволяют применять «зеленые технологии» (электрические автомобили, очищение воды, солнечная энергия, катализаторы).
Сплав с использованием РЗЭ позволяет создавать несущие конструкции, которые можно использовать в самолетостроении, причем при производстве сверхзвуковых моделей. Данные элементы весьма востребованы в космической отрасли. Иллюминаторы, изготавливаемые при добавлении РЗЭ способны выдерживать просто невероятные механические нагрузки.
Отраслевое потребление редкоземельных металлов в мире
| Продукция | 2010 г. | 2015 г. | ||
| тыс. т | $ млн. | тыс. т | $ млн. | |
| Катализаторы | 17,5 | 75 | 16,5 | 66 |
| Полировальные средства | 11,5 | 80 | 20,0 | 50 |
| Стекло | 14,0 | 70 | 12,5 | 47 |
| Сплавы | 12,5 | 75 | 12,5 | 63 |
| Магниты | 10,5 | 130 | 8,0 | 75 |
| Люминофоры | 6,0 | 300 | 4,5 | 158 |
| Керамика | 3,0 | 40 | 2,5 | 30 |
Виды и характеристики
Сами редкие металлы разделены на пять больших групп:
- Лёгкие: бериллий, литий, рубидий, стронций, цезий.
- Радиоактивные: актиний, радий, торий, уран и трансурановые элементы.
- Рассеянные металлы: галлий, гафний, германий, индий, рений, селен, таллий, теллур.
- Редкоземельные: иттрий, лантан и лантаноиды, скандий.
- Тугоплавкие металлы: ванадий, вольфрам, молибден, ниобий, тантал, цирконий.
Данное подразделение весьма условно, так как с совершенствованием геологоразведки и развитием промышленности, некоторые металлы уходят из разряда редких элементов. Само понятие «редкости» говорит об их незначительном использовании. Однако новые прогрессивные технологии коренным образом меняют ситуацию.
Источниками получения редких металлов могут служить месторождения, высокоминерализованные воды, рапа солёных озёр, россыпи, а также побочная продукция или отходы основных производств. Редкометаллические руды можно подразделить на непосредственно богатые редкими элементами, и руды других элементов, в которых редкие минералы присутствуют как примеси. Среди комплексных руд можно выделить:
- вольфраммолибденовые,
- титан-ниобий-тантал-редкоземельные,
- уран-ванадиевые,
- литий-цезиевые,
- цирконий-ниобиевые.
Примерами непосредственно руд редких металлов являются:
- Литиевые руды – это сподумен, амблигонит, лепидолит, циннвальдит, петалит.
- Бериллиевые руды – берилл, бертрандит, фенакит.
- Титановые руды – ильменит, рутил, ильменорутил, перовскит, сфен.
- Циркониевые руды – бадделит, циркон.
9.Лютеций
В виде оксида лютеций был открыт в 1907 году Вельсбахом, Урбеном и Джеймсом. Впервые чистый лютеций был выделен в 60-х годах прошлого века. Получают лютеций из минералов путем ионного обмена, экстракции и восстановления с помощью кальция из фторида лютеция. Цена на этот редкоземельный металл составляет 3-3,5 тысячи долларов за 1 килограмм чистого вещества.
4 стр., 1818 слов
Принцип работы электронного микроскопа
… специализированные электронографы промышленного типа. Кроме того, в некоторых электронных микроскопах предусмотрена возможность работы в режиме электронографии. Следует заметить, что с точки зрения физики … методов имеет свою область применения. Особенности работы с электронным микроскопом Остановимся кратко на основных приемах работы в электронной микроскопии. Естественно, что эти приемы …
Лютеций — метал серебристого цвета, самый тяжёлый в своей группе. Он легко поддаётся обработке. На воздухе этот металл покрывается плотной пленкой из оксида лютеция. Взаимодействует со многими неметаллами и неорганическими кислотами.
Лютеций применяется в производстве лазерных материалов, магнитных сплавов для космической техники, для создания жаропрочной проводящей керамики, в ядерной энергетике. С добавлением лютеция производят сплавы с высокотемпературной сверхпроводимостью, а также составы для легирования жаростойких материалов.
Рисунок 4.4.1 — лютеций
Общие способы получения металлов
Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt,Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
Минералы и черные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами.
Получение металлов из руд — задача металлургии.
Металлургия — это и наука о промышленных способах получения металлов из руд, и отрасль промышленности.
Любой металлургический процесс — это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
М n+ + ne−→M
Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы.
В соответствии с этим существуют следующие способы получения металлов:
• пирометаллургический;
• гидрометаллургический;
• электрометаллургический.
Пирометаллургия
Пирометаллургия — восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов — алюминия, магния.
Например, олово восстанавливают из касситерита SnО2, а медь — из куприта Cu2O
прокаливанием с углем (коксом):
Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
Из карбонатных руд металлы выделяют также путем прокаливания с углем, т. к. карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
Восстановлением углем можно получить Fе, Сu, Zn, Сd, Ge, Sn, Рb и другие металлы, не образующие прочных карбидов (соединений с углеродом).
В качестве восстановителя можно применять водород или активные металлы:
1) МоO3 + ЗН2 = Мо + ЗН2O (водородотермия)
К достоинствам этого метода относится получение очень чистого металла.
2) TiO2+ 2Мg = Тi + 2МgO (магнийтермия)
ЗМnO2 + 4Аl = ЗМn + 2Аl2O3 (алюминотермия)
Чаще всего в металлотермии используют алюминий, теплота образования оксида
https://youtube.com/watch?v=_-nVROAFWAY
которого очень велика (2А1 + 1,5 O2 = Аl2O3 + 1676 кДж/моль). Электрохимический ряд напряжений металлов нельзя использовать для определения возможности протекания реакций восстановления металлов из их оксидов. Приближенно установить возможность этого процесса можно на основании расчета теплового эффекта реакции (Q), зная значения теплот образования оксидов:
Q= Σ Q1 — Σ Q 2 ,
где Q1— теплота образования продукта, Q2 -теплота образования исходного вещества.
Доменный процесс (производство чугуна):C + O2 = CO2, CO2 + C 2CO3Fe2O3 + CO = 2(Fe2Fe32)O4+ CO2(Fe2Fe32)O4+ CO= 3FeO + CO2FeO + CO= Fe + CO2(чугун содержит до 6,67% углерода в виде зерен графита и цементита Fe3C);
Выплавка стали (0,2-2,06% углерода) проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева.
Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов.
При этом оксиды либо улавливаются в виде отходящих газов (CO2, SO2), либо связываются в легко отделяемый шлак – смесь Ca3(PO4)2 и CaSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Гидрометаллургия
Гидрометаллургия — это восстановление металлов из их солей в растворе.
Процесс проходит в два этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СuО, ее обрабатывают разбавленной серной кислотой:
СuО + Н2SО4 = СuSO4 + Н2
Затем медь либо извлекают из раствора соли электролизом, либо вытесняют из сульфата железом:
СuSO4. + Fе = Сu + FеSO4
Таким образом, получают серебро, цинк, молибден, золото, уран.
Электрометаллургия
Электрометаллургия — восстановление металлов в процессе электролиза растворов или расплавов их соединений.
Этим методом получают алюминий, щелочные металлы, щелочноземельные металлы. При этом подвергают электролизу расплавы оксидов, гидроксидов или хлоридов.
Примеры:а) NaCl (электролиз расплава) → 2Na + Cl2
Тантал
Дорогостоящий тантал, получивший свое название в честь персонажа греческих мифов, является редким металлом, который очень сложно добыть в чистом виде. Цвет металла светло-серый.
Тантал используется для изготовления электронных приборов, а также часто применяется в промышленности, наиболее часто — в химической. Редкий металл имеет уникальное свойство – биосовместимость. Благодаря этому тантал используется в медицине. Если из него изготовить протез, то можно избежать отторжения организмом инородного предмета.
Советуем почитать: Аллергия на золото: симптомы и причины появления

Рынок редкоземельных металлов
В настоящее время рынок редкоземельных металлов в упадке, и Китай планирует ограничить годовое производство до 140 000 метрических тонн, начиная с 2020 года, чтобы попытаться снова поднять цены.
Причины падения цен на редкоземельные металлы
Начнем с супермагнитов.
Неодим — редкоземельный элемент, примерно с концентрацией в земной коре, как свинец и хром, но сосредоточен в высокосортных рудах. В 1982 году Дженерал Моторс и японская компания Сумитомо обнаружили, что смешивание одной четвертой неодима по весу с тремя четвертями железа и бора может сделать самое мощное семейство супермагнетиков тогда известным, Nd2Fe14B и что свойства этих магнитов могут быть дополнительно улучшены путем добавления следов других редкоземельных металлов — празеодима плюс диспрозий или более дорогой тербий.
Китай, обладая большим количеством всех этих элементов и предпочитая добавленную стоимость экспорту сырья, создал индустрию супермагнитов, чьи низкие цены захватили большую часть мирового рынка и закрыли конкурентов. Китай также энергично проводит исследования и разработки, чтобы найти дальнейшее применение своей редкоземельной щедрости.
Даже в 2015 году, на долю Китая приходилось более 80% мирового редкоземельного производства, сейчас около 70 процентов — это неразумный баланс.
Технологические решения по уменьшению спроса
С 2010 года промышленники предупредили, что рынок редкоземельных металлов с монополией Китая на элементы супермагнитов могут сделать растущий глобальный переход на электрические автомобили и ветряные турбины невозможным — потому что их двигатели и генераторы якобы требовали супермагнитов и, следовательно, этих элементов. Некоторые такие сообщения были даже в 2017 году. Но это все подвергается сомнению. Все, что делают такие вращающиеся машины с постоянными магнитами, также может быть сделано или лучше двумя другими видами двигателей, которые не имеют магнитов.
Сейчас двигатели применяют современную управляющую программу и силовую электронику из кремния, самого распространенного твердого элемента на Земле.
Первый вид — это асинхронный двигатель, изобретенный Николой Теслой 130 лет назад и используемый в каждом электромобиле Приус и Тесла сегодня. Без магнитов изготавливают двигатели не только в электрических автомобилях, но также в ветротурбинах, что освобождает тонны неодима. То, что некоторые ветряные турбины и производители используют генераторы с постоянными магнитами, не означает, что другие должны их изготавливать также.
Точно также красные люминофоры в компактных люминесцентных лампах традиционно используют европий. Но эти лампы теперь в значительной степени вытеснены белыми светодиодами, которые используют примерно на 96 процентов меньше европия. Кроме того, новые красные люминофоры не используют редкоземельные металлы, в то время как последний зеленый люминофор сокращает использование тербия более чем на 90 процентов.
Эрбий в волоконно-оптических ретрансляторах — еще один редкоземельный элемент. Эрбий необходим чтобы увеличить емкость волокна. Ширина полосы частот сейчас увеличена путем передачи по мултиплексу и беспроволочными рационализаторствами.
Некоторые гибридные автомобили, такие как Honda Insight 2001 года, использовали никель-металл-гидридные батареи, содержащие лантан, но теперь они в значительной степени заменены более легкими литиевыми батареями, которые обычно не используют лантан. Кроме того, электромобилям с литиевыми батареями требуется в два—три раза меньше батарей по массогабаритным характеристикам.
Лидирующие на рынке литиевые батареи электромобиля в мире, как и их двигатели, вообще не используют редкие металлы. Количество электромобилей в мире растет. Появляются новые технологии в виде мощных потенциальных заменителей батарей (в частности, графеновые суперконденсаторы).
Почему используют именно сплавы?
Технику производят из металлических материалов с многочисленными свойствами. Чистейшие и полученные различные способами металлы содержат в себе небольшие следы примесей, но не обладают нужными характеристиками. Чтобы добиться необходимых эксплуатационных свойств, используют сплавы. Они обладают необходимыми физическими свойствами и позволяют производить огромное количество разнообразных изделий. Сплавами называют однородные макроскопические материалы, которые являются двух- и многокомпонентными. Основная доля химических элементов приходится именно на металлы.
Сплавы отличаются собственной структурой. Все сплавы состоят из следующих компонентов:
- основы — один либо большее количество металлов;
- добавки — модифицирующие либо легирующие в небольшом количестве;
- примеси — остаточные вещества природного, случайного либо технологического характера.
Конкретный состав уже обусловлен сплавом и конкретным производимым конечным изделием.

Китай – мировой лидер производства редкоземельных металлов
Китай считается крупнейшим производителем компьютеров, гаджетов и электроники. Это связано не только со значительными достижениями китайской промышленности, но и с наличием крупнейших в мире запасов редкоземельных металлов — 37 процентов от общемировых. При этом доля Китая в мировом производстве этих материалов составляет 63%. При этом Поднебесная пытается продавать их не как сырье, а в виде готовой продукции.
Остальные страны даже близко не подходят к китайским показателям
Если не брать во внимание Китайскую Народную Республику, США, Индию и Россию можно назвать основными производителями редкоземельных металлов. РФ занимает четвертое место в мире
Где в России добывают палладий
Палладий является одним из самых ценных металлов на земле. Он относится к платиновой группе, имеет серебристо-белый цвет. Крупнейшее его месторождение находится в Норильске. Палладий получают путем переработки сульфидных руд таких металлов, как никель, серебро и медь.
Россия добывает более половины от мировой добычи палладия. Правда США закупает его у разных стран — Канады, ЮАР, а также сами добывают на Аляске. Однако Россия покрывает 35% от потребностей страны. Поэтому, в случае наложения ответных санкций, это так же станет серьезной проблемой.
Кроме палладия Россия также может перестать поставлять гелий, фтор и скандий. В результате это может стать серьезным ударом по производству смартфонов, автомобильных запчастей и даже ракет. С учетом того, что на рынке полупроводниковой продукции и так наблюдается дефицит, выпуск данной продукции может быть поставлен под угрозу. Таким образом без высокотехнологичной продукции может остаться не только Россия, но и весь мир.
Разумеется, если США все равно введут санкции, проблему с чипами в России остановка поставок сырья не решит. Собственные заводы должны быть построены только к 2030 году, причем на них будут производиться чипы по 16-нанометровому техпроцессу, который уже сейчас считается устаревшим. К примеру, компания Intel представила Core i9, созданный по 14-нанометровому техпроцессу еще в 2018 году. Поэтому остается надеяться лишь на то, что до введения санкция дело все же не дойдет.
Россия ограничила экспорт инертных газов до конца года
Грязный секрет Apple: разработка РЗЭ в Китае сильно вредит экологии
Думаю, это очевидно, что без китайских РЗЭ производство iPhone просто невозможно. Причем, риск того, что Apple когда-нибудь лишится возможности покупать нужные редкие металлы в Китае, вполне реален
Однако в этом контексте существует еще одна огромная проблема, которую нельзя обойти вниманием. Это влияние добычи РЗЭ в Китае на экологию
Сама Apple очень гордится своей политикой в области охраны окружающей среды. Те пользователи, которых волнует вопрос об экологических последствиях работы компании, могут найти успокоение на сайте Apple, посвященном ее экологической культуре. Там говорится, что производитель iPhone «…без устали трудится над сокращением своего влияния на изменения климата, ищет способы применения экологических материалов и стремится к сохранению ресурсов, которые всем нам нужно беречь». Следующая иллюстрация была создана компанией в доказательство того, что с каждым новым поколением компьютеры Mac потребляют все меньше электроэнергии в спящем режиме.

Эта картинка действительно может заставить нас поверить, что разработки Apple в течение долгих лет, наконец, привели к тому, что сама компания и ее потребители значительно сократили объемы выброса углерода при создании и использовании продукции Apple.
Тем не менее, никто не трубит на каждом углу, что для реализации данной великой цели производитель iPhone увеличил масштабы применения РЗЭ в своих продуктах. Именно за счет этого обеспечивается рост эффективности и производительности работы гаджетов при уменьшении их размеров. Однако цена такой оптимизации кроется в огромном уроне, который наносит китайская индустрия производства РЗЭ окружающей среде.
Те, кто интересуется работой китайской индустрии РЗЭ, могут ознакомиться с трудом Синди Херст «Китайская индустрия РЗЭ: чему может научиться Запад?» (2010). В этой книге есть короткая глава, посвященная серьезнейшим проблемам с экологией, возникающим в данном контексте. В ней автор приводит выдержку из статьи, опубликованной Китайским сообществом редкоземельных металлов.
Госпожа Херст пришла к следующим выводам. Во-первых, производство РЗЭ загрязняет сточные воды настолько, что это наносит ущерб сельскому хозяйству и простым людям в их повседневной жизни. Во-вторых, добыча одной тонны РЗЭ в результате приводит к производству и 2 тыс. тонн отвала (шахтных отходов). В-третьих, радиоактивный торий сбрасывается в Желтую Реку, из которой набирают воду для питья примерно 150 млн человек.

Как же к данной проблеме относятся сами китайцы? Оказывается, для ее решения не делается почти ничего. Китайские компании, в отличие от западных, не отвечают за смерти своих работников по причине экологической опасности. Так что у них нет мотивации для бережного отношения к экологии или для обеспечения более безопасных условий труда для работников (к примеру, предотвращения развития у них пневмокониоза, или запыления легких). Иногда китайских производителей все же побуждают обеспечивать более безопасные условия работы и беречь экологию. Но поскольку земли, на которых функционируют производства, находятся в государственном владении и сдаются в аренду, страх конфискации приводит к совершенно другой позиции. Компании стремятся выжать из земли максимум продукта (и, соответственно, прибылей) за кратчайшие сроки. Конечно, в таких условиях мало кто заботится об окружающей среде.
Так что нашим глазам предстает гораздо более печальная картина, чем та, что рисует Apple для своих инвесторов и потребителей. В этом контексте политика компании из Купертино заключается в расхожей фразе «Я этого не вижу, значит, этого нет».
Отдельная группа элементов
Состоящая из 17 элементов периодической таблицы, группа элементов, известная как редкоземельные металлы обеспечивает значительную ценность для технического и экономического роста. Эти важные элементы используются в высокотехнологичных продуктах как катализаторы, сотовые телефоны, жесткие диски, гибридные двигатели, лазеры, магниты, медицинские службы, телевидение и другие применения.
Это:
• Лантан 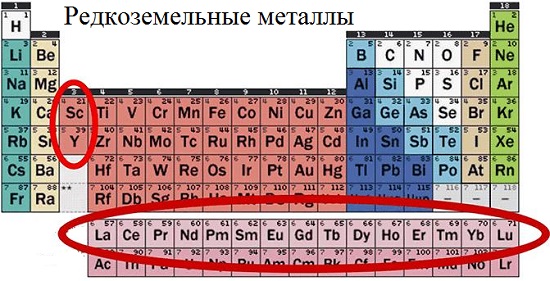
• Церий
• Неодим
• Прадеозим
• Самарий
• Прометий
• Гадолиний
• Европий
• Тербий
• Гольмий
• Диспрозий
• Эрбий
• Иттербий
• Лютеций
• Тулий
• Иттрий.
По данным геологической службы США, в какой-то момент на Китай приходилось 98% мирового производства редкоземельных элементов. В 2017 году этот показатель составлял 85%.
Физико-химические характеристики
Внешне, по физическим и химическим свойствам рений схож с платиноидами:
- Термопрочность. Характеристики, формула не меняются при длительном нагревании до 2000°C, многократных скачках от перегрева к переохлаждению.
- Каталитические характеристики.
- Повышенная стойкость к агрессивным веществам. Растворяется только азотной, нагретой серной кислотой, расплавами щелочей, пероксидом водорода.
- Окисляется при 301°С.
- Образует сплавы, соединения с галогенидами, серой.
| Свойства атома | |
|---|---|
| Название, символ, номер | Ре́ний / Rhenium (Re), 75 |
| Атомная масса (молярная масса) |
186,207(1) а. е. м. (г/моль) |
| Электронная конфигурация | 4f14 5d5 6s2 |
| Радиус атома | 137 пм |
| Химические свойства | |
| Ковалентный радиус | 128 пм |
| Радиус иона | (+7e) 53 (+4e) 72 пм |
| Электроотрицательность | 1,9 (шкала Полинга) |
| Электродный потенциал | Re←Re3+ −0,30 В |
| Степени окисления | от +7, +6, +5, +4, +3, +2, +1, 0, −1 |
| Энергия ионизации (первый электрон) |
759,1 (7,87) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 21,02 г/см³ |
| Температура плавления | 3459 K (3186 °C, 5767 °F) |
| Температура кипения | 5869 K (5596 °C, 10105 °F) |
| Уд. теплота плавления | 34 кДж/моль |
| Уд. теплота испарения | 704 кДж/моль |
| Молярная теплоёмкость | 28,43 Дж/(K·моль) |
| Молярный объём | 8,85 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | Гексагональная (плотноупакованная) |
| Параметры решётки | a=2,761 c=4,456 |
| Отношение c/a | 1,614 |
| Температура Дебая | 416,00 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 48,0 Вт/(м·К) |
| Номер CAS | 7440-15-5 |
Рений – первый по температуре кипения, второй по тугоплавкости (после вольфрама). Четвертый по «тяжести»: впереди только осмий, платина, иридий. По электросопротивлению вчетверо превосходит вольфрам и молибден.
Низкое потребление не стимулирует
В советские времена потребление редких и редкоземельных металлов для высокотехнологической промышленности составляло примерно 8500 тонн. Два года назад было 1160 тонн, сейчас потребление опустилась ниже 1000 тонн. И это, как отметил академик Похиленко, показывает уровень нашей высокотехнологической промышленности. К сожалению, низкое потребление, то есть отсутствие спроса, не стимулирует развитие разведочных работ и добычных компаний по этому направлению.
Рения, металла, без которого невозможно строить двигатели самолетов, в мире производится всего 54 тонны в год, и почти все закупают Штаты. А в России рения производится всего лишь сотни килограммов. Хотя российской промышленности требуется не менее пяти тонн в год
Практически все металлы, что мы производим, констатировал Николай Похиленко, мы вывозим и при этом практически все ввозим в виде готовой продукции. Мы вывозим германий, но ввозим его в виде продукта. Рения, металла, без которого невозможно строить двигатели самолетов, производится в мире всего 54 тонны в год, и почти все закупают Штаты. А в России рения производится всего лишь сотни килограммов. Хотя российской промышленности требуется не менее пяти тонн рения в год. И так со многими металлами.
Оба докладчика согласились с тем, что Россия нуждается в восстановлении геологической отрасли, для чего необходимо создание соответствующей госкорпорации или Министерства геологии. Необходимо увеличить государственные ассигнования на геологию как минимум в три раза. Если этого не сделать, будет сложно обеспечить возобновление ресурсов по широкому кругу твердых полезных ископаемых. И наши планы развития высокотехнологической промышленности будут упираться в серьезные риски, связанные уже с состоянием национальной безопасности. Потому что нам могут что-то не продать из того, что мы сами не нашли и не добываем. Нормальное функционирование таких отраслей, как ракетостроение, самолетостроение, электроника и атомная промышленность, может оказаться под угрозой.
Мировая добыча алюминиевых руд
За последние сто лет уровень добычи алюминиевой руды возрос до невероятных значений. Если в 1913 году общемировой объем породы составлял приблизительно 550 тыс. тонн, то на сегодня этот показатель превышает 190 млн тонн. Около 30 стран сейчас занимаются добычей алюминиевой руды. Лидирующую позицию занимает Гвинея (Западная Африка), где сосредоточено множество месторождений с запасами, равными 28% от мировой доли.

По объемам непосредственно добычи руды на первое место следует поставить Китай. Так, страна «заходящего солнца» за год добывает более 80 млн тонн сырья. Пятерка лучших выглядит следующим образом:
- Китай — 86 млн т;
- Австралия — 82 млн т;
- Бразилия — 31 млн т;
- Гвинея — 20 млн т;
- Индия — 15 млн т.
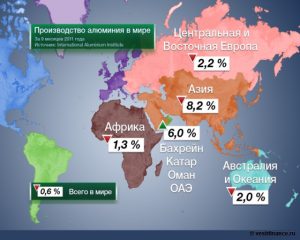 Производство алюминия в мире
Производство алюминия в мире
После следует Ямайка с показателем в 9,7 млн тонн и, наконец, Россия, общий объем добычи алюминиевой руды которой составляет 6–7 млн тонн. Лидеры в алюминиевой промышленности на протяжении многих лет все время менялись.
Впервые руда была добыта во Франции, в местечке Бокс, благодаря чему самый распространенный тип руды называется бокситом. Вскоре лучшими показателями могли похвастать Западная Европа и Северная Америка. Через полвека неоспоримым лидером стала Латинская Америка. Сейчас же вперед выбились Африка, Австралия, Китай и другие развитые страны.
Цветные металлы являются неотъемлемой частью современной промышленности. Без них не было бы возможным развитие множества отраслей. Алюминий, как легкий, прочный и функциональный металл, считается ключевым конструкционным материалом нынешнего времени.
Видео по теме:
Подведение итогов
Металлы, которые используются в производстве различных изделий, не являются чистыми. Большинство добывают в виде руды. Она изымается в карьеры чаще всего подрывным способом и доставляется на перерабатывающий металлургический комбинат. Конкретный метод обработки зависит от разновидности руды.Получаемый в результате металл может быть условно чистейшим, поскольку содержит некоторое количество примесей. Это не делает его пригодным для производства конечных изделий, поскольку материал еще не обладает всеми необходимыми эксплуатационными свойствами. Для изготовления металлической продукции используют сплавы.


































