Содержание:
Карбид для сварки или полное наименование карбид кальция – это главное вещество для получения ацетиленового газа. На самом деле, это активное химическое соединение кальция и углерода и в готовом виде представляет собой твердый состав с темно – серым или коричневым оттенком. По запаху, карбид напоминает резкий запах чеснока и вступает в реакцию водой с выделением тепла.
Для сварки карбид кальция является идеальным веществом, так как выделяет при контакте с водой ацетилен – летучий газ, основа кислородной сварки, напайки, металлизации и прочих процессов, связанных с обработкой металлов. Карбид кальция создают при температуре до 2300 градусов Цельсия с помощью сплавления кокса и негашеной извести в электрической дуговой печи (рис. 1). После этого, расплавленное вещество выливают на изложницы, и в них он остывает и принимает твердое состояние. После этого карбид для сварки дробят по кускам, размер которых не превышает 8 см. В результате вещество будет состоять из 75 процентов карбида кальция, а остальная часть – примеси, окиси извести и прочее.
Карбиды вольфрама W2C и WC
Карбиды вольфрама W2C и WC представляют собой соединения серого цвета. Область температурной устойчивости для W2C составляет до 2750°С; для WC — до 2600°С. Тонкий порошок WC быстро окисляется на воздухе при 500…520°С. Температура начала окисления грубого порошка WC составляет 595°С. При 700°С изменение массы карбида вольфрама WC в результате часового окисления составляет 8,3 мг/(см2·ч).
При комнатной температуре порошок карбида вольфрама практически не растворяется в сильных концентрированных кислотах. Однако он почти полностью растворим в кипящих H2SO4 и HNO3. При температуре 940°С WC слабо взаимодействует с расплавом цинка. Физические свойства карбидов вольфрама W2C, WC
| Свойства/карбид | W2C | WC |
| Молекулярная масса | 379,7 | 195,9 |
| Тип решетки | Гексагональная | |
| Плотность, кг/м3 | 1720 | 1560 |
| Температура плавления, °С | 2730±15 | 2720 |
| Температура кипения, °С | 6000 | |
| Твердость по шкале Мооса | 9-10 | 9 |
| Средний ТКЛР в интервале 20-2000°С, α·106, град-1 | 5,8 | |
| Удельная массовая теплоемкость в интервале 0-100°С, Дж/(кг·град) | — | 184 |
| Молярная теплоемкость при 25°С, кДж/(кмоль·град) | — | 36 |
| Коэффициент теплопроводности при 20°С, Вт/(м·град) | 29,3 | 197 |
Интересные соединения
Карбид натрия. Формула этого соединения C2Na2. Это можно представить скорее как ацетиленид (то есть продукт замещения атомов водорода в ацетилене на атомы натрия), а не карбид. Химическая формула полностью не отражает этих тонкостей, поэтому их надо искать в строении. Это очень активное вещество и при любом контакте с водой очень активно взаимодействует с ней с образованием ацетилена и щёлочи.
Карбид магния. Формула: MgC2. Интересны способы получения этого достаточно активного соединения. Один из них предполагает спекание фторида магния с карбидом кальция при высокой температуре. В результате этого получаются два продукта: фторид кальция и нужный нам карбид. Формула этой реакции достаточно проста, и вы можете при желании ознакомиться с ней в специализированной литературе.
Если вы не уверены в полезности изложенного в статье материала, тогда следующий раздел для вас.

Применение
Как уже упоминалось, чаще всего это вещество можно встретить на стройке. И там ему находят десятки способов применения. В шлифовке без этого материала трудно обойтись, из него производят спец. диски. Но хорош он не только в качестве абразива, но и в виде острых режущих кругов, ножей и тому подобного.
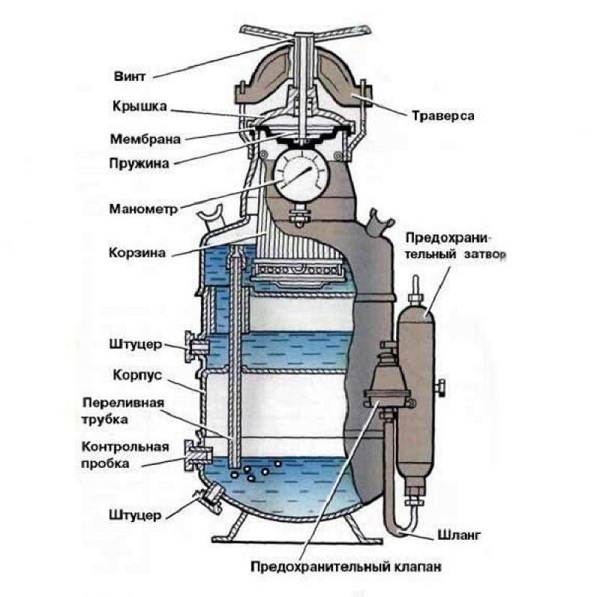
Генератор ацитиленовый для газосварки, внутрь которого засыпается карбид кальция
Машиностроение – еще одна возможность использовать это соединение. Из карбида получаются не только различные детали автомобилей, но и зап. части для радио приборов. А благодаря своей теплопроводности он отлично справится и с задачей нагревательного типа. Даже в ядерной промышленности без такого составляющего никак. Все это требует особой прочности, поэтому здесь речь чаще всего о ковалентных видах.
Те составы, что содержат карбид железа, позволяют получить сталь, и всем известный чугун. Кремниевые соединения так же ценят ювелиры и производители осветительных элементов. Искусственный каучук и смолы, и даже уксусная кислота – настолько широк круг применения карбидов.
Но этим дело не ограничивается. Этот искусственный минерал еще и для огородников важен. Ведь с его помощью получают особый вид удобрений. Они способны регулировать скорость роста различных культур.
Но, пожалуй, самый популярный из всех – карбид кальция. Ведь именно его в своей работе активно используют сварщики. Казалось бы, как этот темный камушек с чесночным ароматом может быть задействован в таком процессе?
Очень просто, ведь для газовой сварки, что логично, нужен горючий газ. В нашем случае дает карбид ацетилен. Как только он «встречается» с кислородом, мы получаем весьма интенсивное пламя, его температурные показатели переступают отметку в три тысячи градусов.
Если брать уже готовый летучий газ, то упаковкой ему служат спец. емкости, в них вещество доставляют к месту действия. Никакой тряски, или ударов во время такой поездки быть не должно – смертельно опасно.
Это сырье может вспыхнуть, даже без лишней «помощи», потому внимание всегда должно быть на пределе. Если же пожара избежать не удалось, никакой влаги при тушении
В ход должны идти только порошковые способы тушения.

Есть второй путь – произвести это «топливо» прямо на месте работ. Для этого нужно знать, что такое гидролиз карбидов. Говоря проще, это реакция соединения на контакт с водой. Причем, этот самую реакцию может вызвать даже одна капля.
Потому, если собрались осуществить сварочные работы, предельно аккуратно вскрываем герметичную тару с карбидом
Особо важно, чтобы никаких признаков огня по соседству, иначе ЧП гарантированно. О сигаретах и вовсе стоит забыть
Еще следите за тем, чтобы даже самые мелкие крошки не оказались на Вашей коже, тем более на слизистых, иначе, в лучшем случае – раздражение, с худшем- ожоги и распухшие части тела. Так что вооружайтесь спец. обмундирование: защитить нужно все, с ног до головы, в том числе и дыхательные пути. Первая помощь, если контакта избежать не удалось: обильно поливаем водой пораженный участок, покрываем его плотным кремом. При необходимости вызвать врача.
Если говорить о расходе, если масса карбида один килограмм, то это дает возможность выработать до трехсот кубических дециметров газа. Это достаточно хорошие показатели. Так же на такое количество сырья потребуется примерно литров 20 воды, хотя производители и заявляют, что достаточно будет полулитра. То, сколько времени все это займет, зависит от величины фракций соединения, и их чистоты.
После того, как с работой закончили, оставшиеся отходы, а это шлак из извести, не оставляем где попало, а утилизируем. Для таких работ потребуется спец. генератор. Бывают они внушительных размеров, их устанавливают на одном месте, к примеру, когда планируются масштабные работы. Но существует и мини-версия, переносная.
Сначала отсек, в котором и должен образоваться газ, заливаем водой, потом уже добавляем туда карбид. Идет реакция, появившийся в результате ацетилен по мягкой трубке поступает непосредственно к газовой горелке. Этот путь должен быть достаточно длинным, шланг обязательно нужно выбрать не короче десяти метров.
Карбид бора
Идет в дело и карбид бора. Предметы на его основе дают надежную защиту от огня. И не только от огня, кстати, ведь такой товар активно используют изготовители бронежилетов. Во-первых, он «ловит» пули, а во-вторых, не даст прохода и радиации. Что касается такого союза, как карбид алюминия, то сверкающие искры во время фейерверков – его заслуга. А ведь на вид это ничем не примечательный желтый порошок.
Карбид: что это такое. Свойства, производство, применение
instrument.guru > Металлообработка > Карбид: что это такое. Свойства, производство, применение
Карбиды металлов — это соединения, которые не являются природными, получают их только искусственным путем.
Первое упоминание о создании этого вещества относится к началу 19 века, его синтезировал англичанин Деви в своей лаборатории. Позже были созданы и другие соединения.
В детстве многие любили взрывать это вещество, но далеко не все понимают, что же представляет из себя это соединение.
- Состав и виды карбидов
- Свойства
- Производство карбида
- Применение в промышленности
- Хранение и транспортировка
- Стоимость
Хранение и транспортировка
Поскольку карбид при вступлении в реакцию с влагой приводит к выделению большого количества тепла и взрывоопасного газа ацетилена, хранят данное вещество в герметичных баках или барабанах
Работа с такими баками требует особой осторожности
Газ ацетилен легче воздуха и способен самовоспламеняться, при этом обладает наркотическим действием.
При вскрытии барабанов с карбидом используют специальный инструмент, исключающий возникновение искр, а при попадании вещества на кожу требуется немедленно промыть водой пораженный участок и смазать жирным кремом.
Помещения хранения должны хорошо проветриваться, а содержание других веществ по соседству — запрещено. Это может привести к опасным реакциям. Неправильное хранение может как взорвать карбид, так и привести его в негодное состояние.
Срок хранения доходит всего до полугода.
Перевозка осуществляется только крытым транспортом. Воздушная доставка запрещена.
Стоимость
А вот, карбид вольфрама обойдется в 1400 рублей за кило. Причем, может быть установлен минимальный вес покупки, например, от 10 кг. Карбид бора будет стоить еще дороже — от 2000 рублей, причем фасовка начинается от 35 килограмм.
Стоимость же соединений с гафнием или молибденом оговаривается с поставщиком отдельно.
Карбид кальция в сварке
Для сварочных работ карбид является чуть ли не идеальным веществом, потому что при взаимодействии с водой выделяет в окружающее пространство летучий газ ацетилен, который служит основой металлизации, напайки, кислородной сварки и множества иных процессов, относящихся к обработке металлических сплавов.

субстанция будет состоять
Так как при воздействии воды карбид выделяет большое количество ацетиленового газа и тепловой энергии, это существенно затрудняет его хранение. Чтобы избежать порчи вещества, его нередко укладывают в герметичные стальные резервуары. При открытии этих металлических сосудов необходимо избегать открытого пламени и искр, иначе могут быть печальные последствия.
https://youtube.com/watch?v=QXp3OIBnSzk
Карбидная пыль (частички до 2 мм) непригодна для применения, потому что растворяется в воде практически моментально. Кроме того, при хранении большого количества пыли увеличивается риск, что применение состава в итоге приведет к взрыву резервуара. Специалисты отмечают, что килограмм рассматриваемого вещества способен выделить при взаимодействии с водой более 260 кубических дюймов ацетилена.
Карбид кальция как «топливо» для сварки.
Как уже было выше сказано, карбид при сварке вступает в активную реакцию с водой, выделяя огромное количество тепла и ацетиленового газа. Эта его особенность усложняет хранение карбида, поэтому для его сохранности вещество помещают в герметичные баки из кровельной стали вместимостью 100 и 130 килограмм
Так как карбид выделяет легковоспламеняющийся ацетилен, то жизненно важно при открытии данных бидонов избежать искр и открытого огня
Пыль карбида кальция – частицы до 2 миллиметров – не годится для использования, так как практически сразу растворяется в воде и при этом, возрастает вероятность, что использование такого состава приведет к взрыву всего баллона.
Для любознательных – один килограмм карбида кальция, в зависимости от чистоты и размера кусков, при контакте с водой может выделить более 250 дм 3 ацетилена!
Карбид кальция активно применяется во время газовой сварки и резки. Во время горения с кислородом, ацетилен может достигнуть наивысшей температуры плавления до 3150 градусов Цельсия, что делает его незаменимым в работе с тугоплавкими металлами, потому что для сваривания или резки необходима температура, вдвое превышающая градус плавления самого металла.
Для безопасного использования, ацетилен производят в специальных генераторах (рис. 2) на основе карбида кальция или природного газа, нефти и угля.
Второй способ получения ацетилена из природного газа, нефти и угля – более дешевый, чем применение карбида кальция, примерно на 30 – 40%.
Техника безопасности при работе с карбидом кальция.
Как уже Вам известно, карбид кальций — это взрывоопасное вещество и для обеспечения безопасной работы с ним необходимо выполнять несколько обязательных правил при использовании карбида для сварки. Главные положения, которые необходимо выполнять при сварочных работах на основе карбида кальция:
Учитывайте, что карбид кальция активно взаимодействует с воздухом и водой, выделяя легковоспламеняющийся ацетиленовый газ
Место хранения карбида для сварки должно быть сухим и герметичным.
Карбид кальция также взрывоопасен, поэтому искры и открытый огонь рядом с веществом строго воспрещены.
Пыль карбида (куски менее 2 мм) вызывают раздражения, попадая на кожу, глаза и слизистую оболочку рта, и носа.
Регулярные сварочные работы с применением карбида кальция должны проводиться в специально оборудованном для сварки помещении, в котором нет горючих веществ, и присутствуют только несгораемые материалы
Жизненно важно, чтобы все оборудование, связанное с хранением и производством ацетилена было изолировано в отдельных отсеках сварочной мастерской, а само помещение для генераторов должно легко проветриваться и в случае чего деактивироваться.
Установка генераторов ацетилена строго запрещена в подвальных комнатах.
После завершения сварочных работ с применением карбида кальция как «топлива», в генераторах все оставшееся вещество дорабатывается, и полученные шлаки в виде известкового ила удаляем из генератора в специальную яму или бункер.
Напомним, что карбид и ацетилен — взрывоопасные вещества. Поэтому курение, открытый огонь на расстоянии до 10 метров от места хранения отработанного карбида строго воспрещено.
При перевозке и хранении ацетиленовых баллонов, на конструкцию клапанов должны быть навинчены предохранительные колпаки
Толчки и удары при транспортировке нескольких баллонов смертельно опасны. Хранение и перевозка ацетиленовых баллонов с другими веществами не допустима.
И напоследок отметим, что карбид кальция является высокоинтенсивным веществом для получения ацетиленового газа, что сводит к минимуму его расход. Кроме того, один килограмм ацетилена, полученного из карбида кальция, выделяет тепла около 8 тысяч кДж.
Карбиды — это соединения металлов и неметаллов с углеродом. Обычно в таких соединениях углерод имеет большую электроотрицательность, чем второй элемент, что позволяет исключить из группы оксиды, галогены и другие углеродные соединения.
Это твердые тугоплавкие вещества, нелетучие и нерастворимые. В основном они обладают разнообразными свойствами: некоторые, например, карбид золота, может взорваться при попытке пересыпать его, а некоторые из соединений, например, бора, циркония, титана, кремния и вольфрама, по твердости превосходят алмаз и не поддаются действию кислот и растворителей.
Это интересно: Что такое курвиметр — характеристики и назначение прибора
Методы получения карбидов
Карбиды могут быть получены взаимодействием углерода и его соединений с металлами или их соединениями. Известны следующие способы получения карбидов: 1) получение карбидов в литом виде;
2) науглероживание порошков металлов (или окислов) твердым углеродом;
3) науглероживание порошков металлов (или окислов) газами, содержащими углерод (часто в присутствии твердого углерода);
4) осаждение из газовой фазы (метод наращивания);
5) химическое выделение карбидной фазы или углеродистых ферросплавов или расплавов (метод растворения);
6) электролиз расплавов соответствующих солей.
Промышленное применение имеют первые три способа.
Получение литых карбидов основано на сплавлении металлов с углеродом и возможно только в электрической или высокочастотной печи, так как температуры образования и плавления карбидов тугоплавких металлов лежат в пределах 2500—4000° С. Это вызывает определенные технические трудности, поэтому способ получения литых карбидов имеет ограниченное применение.
Получение карбидов науглероживанием порошков металлов или окислов металлов твердым углеродом имеет наибольшее распространение и используется для промышленного приготовления карбидов вольфрама, титана, молибдена, тантала, ванадия и других карбидов, применяемых в производстве твердых сплавов.
В качестве исходного сырья при этом способе используют порошки чистых металлов или их окислов. Углерод вводят в смесь в виде тонкого порошка сахарного угля или сажи. Смесь металла (или окисла) с углеродом тщательно перемешивают в шаровых мельницах всухую или мокрым способом. При смешивании металла с твердым углеродом дают от 5 до 10% избытка углерода (по сравнению с теоретическим содержанием его), так как в металлических порошках имеется остаточный кислород, а также для компенсации частичного выгорания углерода в печи.
При использовании смесей окислов металла с углеродом учитывают науглероживающее действие образующейся окиси углерода и применяемого защитного газа. Обычно для реакции достаточно 80—90%-ного количества углерода, которое соответствует уравнению
Науглероживание (карбидизацию) проводят в одну или несколько стадий в электрических или реже в газовых печах. Кроме муфельных печей непрерывного действия, применяют угольные трубчатые печи сопротивления, методические печи с молибденовыми нагревателями и вертикальные трехфазные криптоловые печи, а также высокочастотные печи периодического действия с графитовыми тиглями.
В качестве защитного газа используют водород, окись углерода, метан и смеси этих газов. При получении карбидов волфрама и молибдена в качестве защитного газа можно использовать генераторный газ или диссоциированный аммиак.
Реакция науглероживания при образовании монокарбидов протекает по следующим уравнениям:
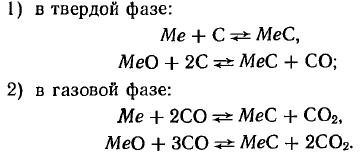
Температура реакции науглероживания металлов с твердым углеродом в зависимости от вида карбидов лежит в пределах 1200—2200° С. В табл. 10 приведены температуры реакций получения наиболее важных карбидов из металлов или окислов при науглероживании твердым углеродом в присутствии углеводорода.
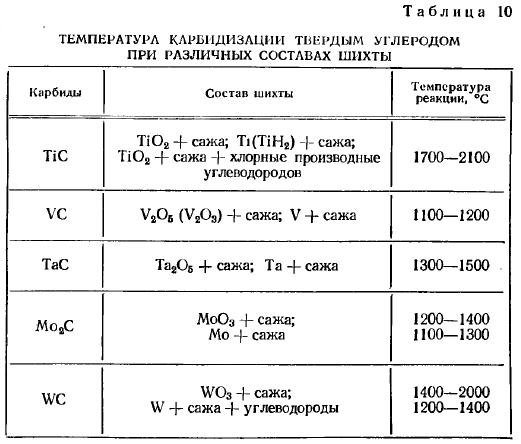
Карбиды молибдена, вольфрама и тантала лучше всего получать науглероживанием металлических порошков сажистым углеродом при температуре 1200—1600°С.
Вольфрам образует два стойких при комнатной температуре карбида: W2C и WC. При науглероживании в твердом состоянии образуется преимущественно монокарбид вольфрама WC, при науглероживании в расплаве образуется W2C. Металлокерамические твердые сплавы содержат исключительно монокарбид вольфрама.
Карбид титана готовят из смеси возможно более чистой двуокиси титана с газовой сажей при температуре 1700—2100° С.
Получение карбидов науглероживанием металловили окислов углеродсодержащими газами. Выше было показано, что при карбидизации в твердом состоянии науглероживание частично происходит и через газовую фазу. В связи с этим возможно получение карбидов науглероживанием исключительно через газовую фазу. Для этого обычно используют металл и углеводород, в результате реакции получают карбид металла и водород. Газовая карбидизация металлов происходит при более высокой температуре.
Науглероживание окислов углеродсодержащими газами проводится редко.
Процесс получения ацетилена из карбида
Устройство для получения ацетилена из карбида кальция называется ацетиленовый генератор. Оборудование бывает передвижным и стационарным. Мобильные генераторы используются, в основном, при проведении ремонтных работ, стационарные — на объектах с большими объемами сварочных процессов. Как получают ацетилен из карбида кальция? Принцип работы генератора состоит в следующем:

- Камера, предназначенная для газообразования, заполняется водой в расчетном объеме.
- Необходимое количество карбида кальция загружается в газообразующую камеру через специальный бункер. Запрещается использовать карбидную пыль, поскольку она может привести к мгновенному выделению газа и разгерметизации аппарата.
- Подача карбида для сварки из бункера в камеру происходит порциями в автоматическом режиме.
- По мере подачи каждой порции давление внутри камеры возрастает. Его снижение служит командой для загрузки последующей части карбида.
- В процессе взаимодействия карбида кальция с водой и происходит выделение ацетилена, который через отборник подается в шланг, ведущий к сварочной горелке.
Вторичный продукт в виде гашеной извести удаляется из генератора при помощи специального бункера. При работе с ацетиленовым генератором надо помнить, что в непосредственной близости от него категорически нельзя курить и пользоваться электрическими инструментами. Газовая горелка должна находиться не ближе 10 метров. Именно такого размера должна быть минимальная длина сварочного шланга.
Если возникла потребность в сварочных работах и нужно решить, где взять карбид, то надежнее всего обратиться к прямым поставщикам или купить в интернет магазинах, которые организуют доставку транспортной компанией.
Карбиды металлов — это соединения, которые не являются природными, получают их только искусственным путем . Первое упоминание о создании этого вещества относится к началу 19 века, его синтезировал англичанин Деви в своей лаборатории. Позже были созданы и другие соединения. В детстве многие любили взрывать это вещество, но далеко не все понимают, что же представляет из себя это соединение.
Как применять карбид против кротов
Карбид кальция в упаковке
Имеется несколько способов, как использовать карбид:
- Просто заложить несколько кусков карбида в кротовую нору и оставить до начала реакции;
- В пластиковые бутылки поместить комковой карбид и налить воды. Закопать эти емкости в норки. Выделившийся ацетилен прогонит кротов раз и навсегда;
- Некоторые садоводы-любители прибегают к более жестким мерам. После выделения газа в норах, его поджигают, обезжизнивая животных.
Но эти меры не всегда помогают избавиться от навязчивых зверьков-вредителей.
Возможно Вам будет интересно — Инструкция по применению гипохлорита кальция для дезинфекции
Преимущества и недостатки метода
Карбид является отличным стимулятором роста некоторых растений. Это, пожалуй, единственное преимущество данного вещества. В основном от него одни недостатки:
- Популяция кротов гибнет, причем особи страдают мучительной смертью.
- Повышается уровень щелочи в почве.
- Уничтожаются живые организмы, обитающие в земле (черви, жуки).
- Высокая опасность возникновения пожара.
Поэтому прежде чем выбрать данный способ борьбы с животными, нужно ознакомиться с имеющимися альтернативными путями. Их очень много: ветряки, консервные банки, отпугиватели из полторашек.
Еще стоит отметить, что крота легко прогнать с огорода, если он непосредственно окажется рядом с карбидом, иначе это пустая трата времени и сил.
Первые признаки авитаминоза. Главные признаки нехватки витаминов, необходимых нашему организму
Витамины и полезные вещества являются необходимыми составляющими для правильного функционирования организма. Человек состоит из множества мельчайших кирпичиков – клеток. Клетки эти имеют определенную структуру, отличаются в зависимости от расположения и предназначения.Все вместе, они образуют ткани, например мышечная, нервная. Ткани образуют органы и системы органов. Взаимодействуя между собой, с помощью сложных биохимических реакций, образуют сложнейшую структуру – человеческий организм. И вот, как раз для правильного и долгого функционирования этой сложной биологической конструкции, необходимо поступление витаминов и полезных веществ извне.
Даже если вы ведете здоровый образ жизни и соблюдаете сбалансированное питание, организму может не хватать отдельных микроэлементов и биологически активных веществ. Более того, соблюдать сбалансированное питание современному человеку очень сложно. Продукты, которые составляют его сегодняшний рацион, оставляют мало шансов для обеспечения организма витаминами и другими полезными веществами в полной мере.
Так, например, сорванные помидоры или бананы, не сразу попадают к нам на стол. Для того, чтобы привезти нам овощи и фрукты из далеких стран «товарного» вида, их срывают зелеными. Соответственно, такие продукты не успевают накопить в себе достаточное количество полезных веществ. Рафинирование продуктов или их термическая обработка тоже существенно снижают в них наличие полезных веществ.
Говоря о витаминной недостаточности, нельзя сказать, что организму не хватает какого-либо одного витамина. Как правило, происходит нехватка группы полезных веществ. Например, если в вашем рационе мало растительных продуктов, ваш организм может испытывать дефицит витаминов В и С. А если отказаться от продуктов животного происхождения, то в организме может наблюдаться недостаточность витаминов А, D и Е.
Признаки витаминной недостаточности
Нехватку витаминов можно определить иногда самостоятельно. Например, недостаток витамина А (ретинол) характеризуется сухостью кожи, ломкостью волос, появлением поперечных полосок на ногтях, заболеванием глаз, куриной слепотой (снижение зрения в темноте), гастритом, диареей, а у детей – замедлением физического и интеллектуального развития. О нехватке витамина Е (токоферола) могут говорить повышенная проницаемость и ломкость капилляров, мышечная слабость, анемия.
Недостаток витамина D (кальциферол) может проявляться в судорогах, нарушении психомоторных реакций, склонности к переломам костей и их медленном срастании. Недостаточность витамина D в детском возрасте может послужить появлению рахита. При этом заболевании нарушается костеобразование и происходит деформация скелета.
Если у вас общая слабость, быстрая утомляемость, частые простуды, кровоточивость десен и плохое заживление ран и порезов – у вас может быть недостаток витамина С (аскорбиновая кислота). О недостатке витамина В1 (тиамина) говорит раздражительность, ухудшение аппетита и сна, мышечная слабость, изменения психики.
Характерными признаками нехватки витамина В2 (рибофлавина) могут стать трещины на губах и в углах рта, ощущение «песка в глазах», светобоязнь, нарушение восприятия различных цветов. Недостаток витамина может вызвать анемию.
Из-за недостатка витамина В5 (пантотеновой кислоты) появляются шелушение кожи, поседение и выпадение волос, усталость, упадок сил. Так же могут появляться желудочно-кишечные расстройства. При появлении подобных симптомов следует обратиться к врачу
Будьте внимательны к состоянию своего здоровья и всегда обращайте внимание даже на незначительные проявления отклонений от нормы.
заместитель начальника Ефремовского территориального отдела Управления Роспотребнадзора по Тульской области Илюхина Светлана Юрьевна
Применение
Область применения карбида кальция чрезвычайно широка. В первую очередь это промышленный синтез. Карбид кальция используется для производства синтетического каучука, уксусной кислоты, ацетона, этилена, винилхлорида, стирола. Также он находит применение в получении цианамида кальция. Это вещество ценно своим использованием в синтезе различных удобрений и цианистых веществ. В сельском хозяйстве любому агроному известно такое название, как карбидно-карбамидный регулятор. Он применяется для регуляции роста растений. А для его получения также используется карбид кальция. Кроме того, это соединение находит применение в процессе производства цианамида кальция. Эта реакция основана на нагревании карбида кальция с азотом. Восстановление щелочных металлов также не обходится без применения описываемого нами вещества. Карбид кальция применяется и в процессе газосварки. Например, широко используются карбидные лампы. Принцип их работы основан на взаимодействии в специальной емкости карбида с водой и сгорании на выходе из аппарата конечного вещества реакции – ацетилена. Посмотрите на фото карбидной лампы.

Область применения карбида кальция [ править | править код ]
Карбид кальция используют при проведении автогенных работ и освещения, а также в производстве ацетиленовой сажи и продуктов органического синтеза, из которых главным является синтетический каучук.
Карбид кальция применяют в производстве цианамида кальция, из которого получают удобрения, цианистые соединения. Карбид кальция используют для получения карбидно-карбамидного регулятора роста растений, изготовления порошкового карбидного реагента.
Из 1 кг технического карбида получается от 235 до 285 л ацетилена в зависимости от его сорта и грануляции: чем чище и крупнее карбид кальция, тем большее количество ацетилена он даёт при разложении.
Для разложения 1 кг карбида кальция теоретически требуется 0,56 л воды. Практически берут от 5 до 20 л воды с целью лучшего охлаждения ацетилена и обеспечения безопасности при работе. Скорость разложения карбида кальция водой зависит от его чистоты, грануляции, температуры и чистоты воды. Чем чище карбид кальция, меньше размер его кусков, выше температура и чище вода, тем больше скорость .
Карбиды – это группа неорганических соединений углерода с металлами, а также с кремнием или бором (поскольку эти элементы проявляют металлические свойства). Карбид кальция – одно из наиболее востребованных веществ этой группы. О свойствах и применении соединения читайте ниже.
Что такое карбид?
Самодельные бомбы. Вот, что приходит на ум первым делом, когда слышим слово карбид. И нет, занимались производством этих опасных игрушек не предприятия оборонной промышленности, а, как правило, мальчишки, лет так десяти.
Лет двадцать назад это было излюбленное развлечение у подростков. Это сейчас все сидят за своими планшетами, а тогда миром правил пытливый ум ребенка, который норовил все испробовать на практике.
Для того, чтобы почувствовать себя Рембо, требовалось раздобыть один чудо-камешек. Находили их дети чаще всего на стройках. А дальше все было просто: пластиковый сосуд, камень, вода, плотно закрученный колпачок. Все это рьяно трясли, и в лучшем случае, отбрасывали куда подальше. А в худшем «снаряд» разрывало прямо в руках, тогда травм было не избежать.
Читать также: Кнопочный пост на 2 кнопки схема подключения
Были и более безопасные пути использовать находку, к примеру, просто бросить в лужицу, тогда можно было наблюдать нечто похожее на действие современных бомбочек для ванны. Так что это за популярная «игрушка». Большинство из нас считали, что таким, как мы его знаем, карбид произвела природа. Но на самом деле это не так. И сегодня Вы в этом убедитесь.
Итак, вещество это всегда очень твердое, плюс ко всему, чтобы его расплавить, нужно приложить недюжинные усилия. На вид это темные, светлые, зеленоватые камни, либо порошок, все зависит от состава. Срок его годности недолог, как правило это полгода. Уложить емкости в общий склад не получится, у таких потенциально опасных веществ должен быть свой отсек.
Как Вы уже знаете, карбид постоянно норовит взорваться. Причем, некоторым соединениям даже особых условий не надо. Достаточно просто пересыпать порошок из тары в тару, как он может неожиданно рвануть.
Как выглядит карбид?
Чтобы определить, где найти карбид на улице, нужно знать его физические свойства. Физически вещество является твердым, его цвет может быть темным, имея сероватый или коричневый оттенок. Цвет зависит от количества углерода. Также имеется специфический запах, который характеризует данное вещество.

По консистенции он твердый, но легко крошится, превращаясь в порошок. Если поднести спичку, то начнется горение с выделением углерода и разложением кальция. Правда, этого можно достичь при высоких температурах, например охотничьей спичкой.
Применение в промышленности
Карбид кальция является важным соединением для получения ацетилена, газа, который используется при кислородной сварке и обработке металлов. При горении с кислородом ацетилен способен достигать 3150 градусов Цельсия. Это позволяет работать с тугоплавкими металлами, требующими температуру вдвое большую,чем температура плавления самого металла.
Карбид бора используется как огнеупорный материал, поскольку температура плавления такого соединения выше 2400 градусов. При этом он же встречается в бронежилетах,так как способен защитить не только от пуль и осколков, но и от радиации. Для покрытия промышленного и строительного инструмента используют карбид титана. Его прочность позволяет повысить износостойкость деталей и обрабатывать даже самые прочные материалы.
Читать также: Метрическая и трубная резьба отличия

































